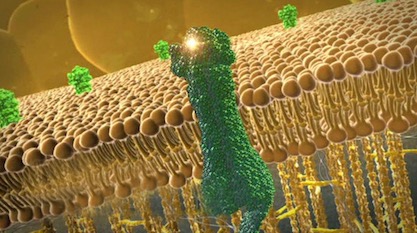
Una diferencia clave entre la vida y lo inerte es el transporte activo. A diferencia de la ósmosis o difusión natural, que tiende a mover moléculas de zonas de alta concentración a zonas de baja, el transporte activo se logra mediante máquinas moleculares capaces de reconocer y permitir el paso selectivamente, incluso contra un fuerte gradiente de concentración. Como el demonio de Maxwell, los canales de membrana parecen violar las leyes de la física. Ninguna ley se viola, por supuesto, como tampoco las puerta giratoria de control de acceso de Disney World violan la física para impedir el paso a quienes no han comprado una entrada. En ambos casos, es la programación y la ubicación de piezas específicas lo que permite que los mecanismos actúen en contra de lo que, de otro modo, ocurriría sin la dirección de la naturaleza.
La mejora en la calidad de las técnicas de imagen permite a los científicos profundizar en los mecanismos de los canales de membrana. Cada canal funciona de forma distinta. Todos tienen algún tipo de «filtro de selectividad» para permitir el paso de las moléculas deseadas y excluir otras. A continuación, se presentan algunos nuevos descubrimientos.
El gran canal de potasio
Biofísicos de la Universidad de Massachusetts en Amherst han descifrado el filtro de selectividad de un tipo de canal iónico: el canal de potasio grande (BK). Este canal opera con gran rapidez en las células musculares y nerviosas. Cadenas de estos canales en la membrana celular se activan en rápida sucesión, creando una onda de información que puede pasar del dedo del pie golpeado al cerebro en una fracción de segundo. Los científicos esperaban que este canal operara una especie de puerta que se abre y se cierra, como en otros tipos de canales. Pero hasta ahora, les desconcertaba por qué el gran poro central del canal parecía permanecer abierto, incluso cuando no entraban átomos de potasio.
Este enigma llevó al equipo de la UMass a descubrir un mecanismo completamente nuevo, denominado «deshumectación hidrofóbica», que es «drásticamente diferente de lo observado en otros canales iónicos». Un cambio en la unión del calcio en el canal hace que las moléculas de agua se aglomeren como en una superficie aceitosa. «Cuando el poro BK es aceitoso, el agua forma una fase de vapor que actúa como una barrera y evita que entren todos los iones», dice Jianhan Chen, miembro del equipo que resolvió el rompecabezas, utilizando modelos computacionales probados con estudios de mutagénesis del mundo real.
Dice: «Si pensamos en por qué la naturaleza querría usar una barrera de vapor donde hay un poro grande que debe transportar mucha corriente eléctrica, para aplicar una barrera física se necesitaría una reorganización estructural de las proteínas que probablemente sería demasiado grande o demasiado lenta, o ambas cosas. En cierto modo, la naturaleza es muy inteligente al usar este fenómeno de deshumectación hidrofóbica para crear una puerta sensible y rápida. Nos sorprendió mucho ver que los cambios en la forma del poro y las propiedades de la superficie son relativamente pequeños y sutiles, pero tienen importantes consecuencias en sus propiedades de hidratación». [Énfasis añadido].
El artículo de investigación de acceso abierto, en Nature Communications, expresa sorpresa por este mecanismo único pero muy efectivo:
El mecanismo de activación de los canales iónicos transmembrana es crucial para comprender cómo estas proteínas controlan el flujo iónico a través de las membranas en diversos procesos fisiológicos. Los canales de potasio grandes (BK) son particularmente interesantes, con una alta conductancia monocanal y una doble regulación por el voltaje de membrana y el Ca2+ intracelular. Las estructuras atomísticas recientes de los canales BK no lograron identificar características estructurales que pudieran bloquear físicamente el flujo iónico en estado cerrado. En este trabajo, demostramos que la activación de los canales BK no parece requerir una puerta física. En cambio, los cambios en la forma del poro y la hidrofobicidad superficial en el estado libre de Ca2+ permiten que el canal experimente fácilmente transiciones de deshumidificación hidrofóbica, lo que genera una gran barrera de energía libre para la permeación de K+.
El canal de protones dependiente del voltaje
Otro canal iónico llamado HV1, vital para la salud de todo, desde las ascidias hasta los humanos, es capaz de discriminar protones. «La activación del HV1 es evidentemente más compleja de lo que imaginábamos», concluye Thomas E. DeCoursey en una revisión de investigación en las Actas de la Academia Nacional de Ciencias (PNAS). Analiza hallazgos recientes de dos estudios sobre el HV1 que parecen indicar que se producen cambios conformacionales coordinados entre las subunidades del filtro de selectividad antes de que pueda pasar un protón. Esta «activación cooperativa» sugiere que «cada canal debe experimentar múltiples transiciones dependientes del voltaje entre estados cerrados antes de abrirse». No debería sorprender que un canal capaz de controlar el paso de iones de hidrógeno atómicamente pequeños deba operar con la máxima precisión y cuidado. Por cierto, DeCoursey señala que una sola célula eosinofílica en el torrente sanguíneo tiene hasta 40.000 de estos canales HV1.
El uniportador mitocondrial
Este canal, presente en las membranas mitocondriales, debe discriminar entre calcio (Ca) y manganeso (Mn), que se encuentran a tan solo 5 números atómicos de distancia en la tabla periódica. Si el uniportador no logra discriminar entre sus iones con doble carga (Ca2+ y Mn2+), puede producirse toxicidad por manganeso, implicada en discapacidades neurodegenerativas como la enfermedad de Parkinson.
El Ca2+ activa la maquinaria del uniportador, según un equipo de siete personas, principalmente del Instituto Médico Howard Hughes y Harvard, en un informe publicado en PNAS. Observe la complejidad irreducible necesaria para dotar a este importante canal de transporte de su exquisita selectividad y capacidad para resistir un pronunciado gradiente de concentración de iones no deseados:
El uniportador mitocondrial es un canal de Ca2+ activado por Ca2+ en la membrana interna del orgánulo. Presenta una conductancia y una selectividad iónica notablemente altas. Es capaz de discriminar entre Ca2+ y otros cationes, incluso aquellos que son de tres a seis órdenes de magnitud más abundantes, como K+ o Mg2+. Normalmente, la selectividad iónica de la conductancia en los canales de Ca2+ se consigue mediante el filtro de selectividad, un estrecho pasaje en el poro del canal que contiene aminoácidos ácidos preparados para quelar el ion conducido. Esta selectividad del uniportador se debe a un motivo «DXXE» altamente conservado, ubicado en el vértice del poro que da al espacio intermembrana. Sin embargo, para el uniportador mitocondrial, el calcio no solo es el ion transportado, sino que también actúa como ligando regulador al activar las manos EF de la subunidad reguladora MICU1 del uniportador. En principio, y como demostramos en este artículo, la selectividad iónica en el sitio de activación del ligando puede contribuir significativamente a la selectividad iónica general del complejo del canal.
Este canal debe permitir la rápida conducción del calcio, pero resistir el manganeso. ¿Cómo lo logra? «Concluimos que la notable capacidad del uniportador para discriminar entre Ca2+ y Mn2+ reside, en parte, en el complejo regulador MICU1-MICU2».
Experimentos con el nematodo de laboratorio C. elegans demostraron que el regulador MICU1 puede unirse a cualquiera de los iones, pero solo el ion calcio desencadena un cambio conformacional. Por lo tanto, actúa como punto de control para asegurar que el manganeso no pase:
En el presente estudio, hemos demostrado que MICU1 proporciona un punto de control que permite al complejo uniportador mitocondrial discriminar entre Ca2+ y Mn2+. En ausencia de MICU1, tanto Mn2+ como Ca2+ pueden pasar libremente a través del uniportador, ya que la conductancia no es altamente selectiva para Ca2+ sobre Mn2+ y se pierde la selectividad de entrada del uniportador. En el holocomplejo, el transporte de Mn2+ se bloquea a menos que el Ca2+ interactúe con las manos EF de MICU1 para inducir una transición conformacional específica.
Conclusión
Este fue solo un breve vistazo a tres mecanismos diferentes en tres canales distintos que facilitan el transporte activo. Existen docenas de familias de canales, que en conjunto ofrecen cientos de máquinas moleculares diferentes, vitales para la vida.
Una célula que no puede controlar lo que entra o sale de su interior no puede sobrevivir. La ciencia debería rechazar todas las hipótesis poco realistas que imaginan simples bolsas de moléculas intentando convertirse en células. Oparin lo intentó en la década de 1920, y algunos intentan mantener vivo su sueño (Astrobiology Magazine). Si la célula más simple concebible requiere canales tan complejos como estos, ¿qué cabe esperar de los demás requisitos, como un código genético, el metabolismo y una membrana? Claramente, mecanismos tan complejos, trabajando todos juntos en armonía, están muy, muy lejos del alcance del azar. Los «conjuntos funcionales» coordinados y jerárquicamente organizados, como los llama Douglas Axe en su libro Undeniable, son sellos distintivos del diseño inteligente.
Crédito de la imagen: Illustra Media, de Origen: diseño, azar y la primera vida en la Tierra.
Artículo publicado originalmente en inglés por Evolution News & Science Today