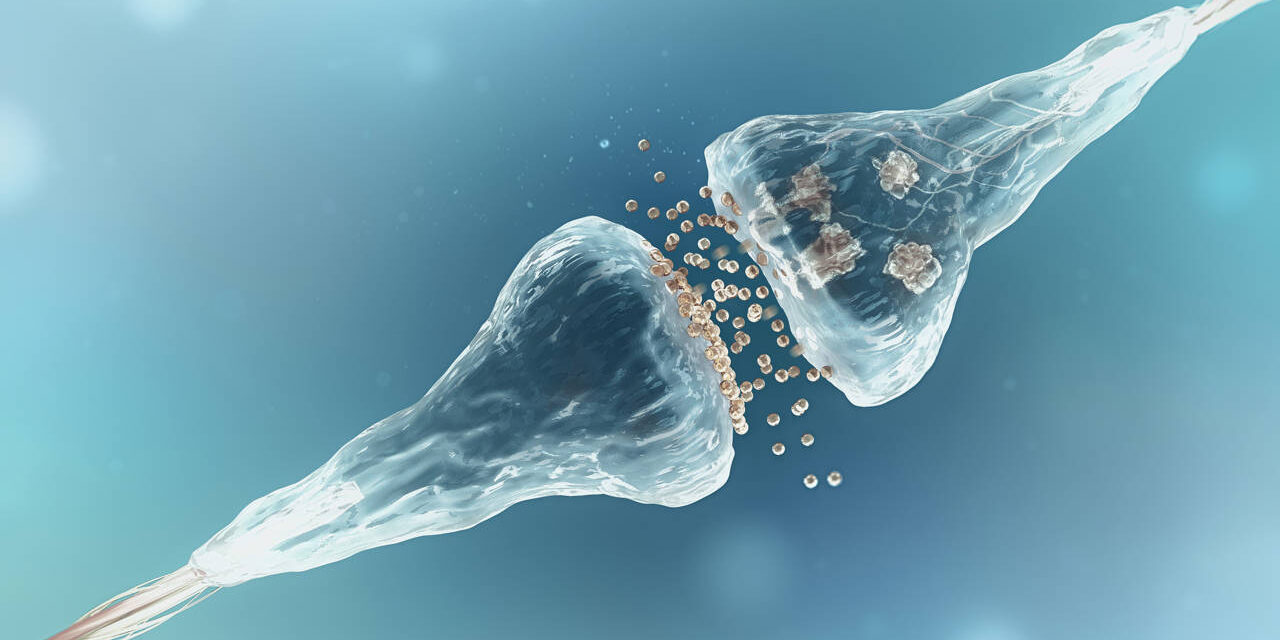
Tras examinar minuciosamente artículos y trabajos científicos, la complejidad de la transmisión sináptica me desconcierta. Que una señal neuronal complete los pasos de empaquetar neurotransmisores, enviarlos a través de un espacio y luego desencadenar una respuesta dentro de la siguiente neurona, parece innecesariamente complicado. Docenas de proteínas y factores intervienen en cada cruce sináptico.
¿Por qué la evolución, o el diseño inteligente, habrían optado por un método así? Parece una chapuza. Las líneas eléctricas que construyen los ingenieros no funcionan así. Mantienen un contacto continuo para el flujo ininterrumpido de electrones. No tendría sentido convertir la electricidad en energía química en cada polo eléctrico y viceversa. ¿Por qué lo hace el cuerpo?
Pero hay que admitir que funciona muy bien y con una rapidez extrema. En cuestión de milisegundos, una señal del pie llega al cerebro y regresa. En su camino, esa señal experimenta repetidamente la conversión de energía en cada sinapsis. Las señales de los pies recorren continuamente casi dos metros de fibras nerviosas repletas de máquinas moleculares y bombas de iones, cruzando sinapsis en cada unión. Es asombroso, pero eso es lo que han descubierto biofísicos y bioquímicos. ¡Profesores de la UC Santa Bárbara estiman que algunas señales neuronales pueden viajar a más de 160 kilómetros por hora!
Como ávido senderista y mochilero, a menudo he cruzado arroyos, caminando sobre troncos estrechos sobre aguas turbulentas. He saltado de roca en roca para superar un montón de rocas, teniendo que decidir en cada momento dónde colocar los pies, adaptándome rápidamente si sentía que la roca se movía. El flujo de información de los ojos al cerebro, a los pies y viceversa, que me proporciona una retroalimentación rápida y continua sobre mi camino, es algo por lo que estoy enormemente agradecido. Esas sinapsis me han proporcionado experiencias vigorizantes y me han salvado de caídas desagradables innumerables veces. Los movimientos rápidos y arriesgados de gimnastas, practicantes de parkour y ardillas superan con creces mis proezas, pero cualquiera que haya recorrido caminos irregulares, subido y bajado escaleras o esquivado rápidamente un objeto en movimiento tiene motivos para interesarse en cómo el cuerpo logra la señalización rápida a través de las neuronas. Ahora, la criomicroscopía electrónica (crio-EM) ha permitido a los científicos profundizar en los misterios de la sinapsis.
Avance del conocimiento
La función básica de la sinapsis se conoce desde hace muchos años. Las moléculas de neurotransmisores, generalmente glutamato (el anión del aminoácido ácido glutámico), se empaquetan en vesículas sinápticas (VS) con proteínas COPI, como pájaros en una jaula. Este proceso es complejo en sí mismo, como describí en mi artículo sobre coatómeros anterior. Activadas por ráfagas de iones de calcio, las VS se unen a la membrana que da a la hendidura y liberan sus neurotransmisores en el espacio. Las moléculas se unen a los receptores del lado receptor, activando otra cadena de canales iónicos que continúan la señal a lo largo de la neurona. La señal se propaga hasta la siguiente sinapsis.
Esto ya se sabía, pero existían muchas preguntas. Los bioquímicos han tenido una capacidad limitada para visualizar los detalles de la hendidura sináptica de 20 nanómetros y los receptores neuronales adyacentes. En PNAS, Richard G. Held y sus colegas de Stanford describieron cómo observaron vesículas sinápticas a escala nanoscópica mediante criotomografía electrónica tras cortar sinapsis del hipocampo con fresado de haz de iones focalizado. Esto les proporcionó una visión sin precedentes de la posición de numerosas proteínas durante el movimiento de neurotransmisores a través de la sinapsis. Efectivamente, las vesículas sinápticas parecen pequeñas bolas con anclajes proteicos para guiarlas.
Haciendo Zoom
Jeremy S. Dittman, de Cornell, comentó el artículo en PNAS. Resumió lo que sucede en preparación para atravesar la sinapsis:
Muchas de las grandes preguntas que actualmente exploran los biólogos sinápticos se centran en los detalles mecanísticos del proceso exocítico y en cómo ambos lados de la sinapsis coordinan la transmisión y la recepción de señales. Brevemente resumidas a continuación: En el lado presináptico, pequeñas vesículas sinápticas (VS) llenas de neurotransmisores se dirigen a la región electrodensa de la membrana plasmática orientada hacia la hendidura, denominada «zona activa» (ZA), donde se unen firmemente a la membrana mediante un conjunto central de proteínas (un proceso denominado acoplamiento y cebado vesicular). Tras la llegada de un potencial de acción y la posterior apertura de los canales de Ca2+ dependientes de voltaje (VGCC abreviado en inglés) presinápticos, el Ca2+ elevado desencadena la fusión de algunas de estas VS preparadas con la membrana plasmática en una fracción de milisegundo, transmitiendo rápidamente una señal química a través de la hendidura. [Énfasis añadido].
Todo esto ocurre en una fracción de milisegundo. Piénsenlo bien.
Una reserva local de vesículas sinápticas (SV) reabastece las vesículas listas para su liberación en una escala de tiempo inferior a un segundo para mantener la actividad sináptica. Justo después de la fusión, el bolo de neurotransmisor se disipa rápidamente dentro de la hendidura mediante difusión, unión a transportadores y, en algunas sinapsis, degradación enzimática.
Los neurotransmisores solo tienen un breve periodo de tiempo para unirse a uno de los receptores de la neurona receptora, generalmente los receptores AMPA. Las señales son recibidas por una región densa en proteínas llamada densidad postsináptica (PSD).
Held et al. querían saber si los neurotransmisores siguen una ruta directa desde la ZA hasta el receptor, en lo que se ha denominado una «nanocolumna» (NC). La sorprendente respuesta fue: algunos lo hacen, pero otros no. Una vesícula sináptica proximal a la membrana (VSPM) suele viajar directamente a un receptor AMPA, pero podría viajar oblicuamente a otro, o a un receptor diferente, como el NMDA. Este mecanismo posiblemente permite transmitir información adicional a la neurona receptora.
Independientemente de si los receptores AMPA se agrupaban en nanoagrupaciones de PSD o se distribuían aleatoriamente a lo largo de la membrana postsináptica, la respuesta promedio a la fusión de una MPSV (número medio de receptores AMPA abiertos) fue similar. Por el contrario, la variabilidad entre cada simulación de MPSV aumentó cuando los receptores AMPA se agruparon en lugar de distribuirse uniformemente. Una implicación de esta simulación es que, suponiendo que los receptores AMPA adoptan una disposición agrupada dentro de la PSD, algunas SV tienen un mayor impacto postsináptico que otras. Dadas las observaciones previas de que las NC en estas sinapsis pueden verse alteradas por la plasticidad sináptica, quizás la falta de correlación entre las MPSV y las nanoagrupaciones de PSD observada en este estudio proporcione un sustrato para aumentar la fuerza sináptica mediante el ajuste de la alineación entre las MPSV y las agrupaciones de receptores de PSD. Combinados con propuestas previas para mejorar la agrupación de los receptores AMPA en respuesta a la inducción de plasticidad, estos efectos podrían aprovechar la variabilidad observada en las simulaciones de Held et al. para producir una mejora significativa en la fuerza sináptica.
Para quienes estén interesados en profundizar en los detalles, el artículo y el comentario mencionan los nombres de numerosas proteínas implicadas en esta rápida transferencia de información a través de la sinapsis. Los autores concluyen con una declaración sobre el ajuste fino:
En conjunto, nuestros datos respaldan un modelo en el que la fuerza sináptica se ajusta a nivel de vesículas individuales mediante la relación espacial entre los nanogrupos de andamiaje y los sitios de fusión de vesículas sinápticas individuales.
Aunque Dittman quedó impresionado por el trabajo, se da cuenta de que deja muchas preguntas:
¿Cómo se organizan los complejos proteicos de ZA para acoplar la elevación de Ca₂+ a la exocitosis en una escala temporal tan rápida? En relación con esto, ¿existen sitios específicos en ZA donde las VS se acoplan, se preparan y se fusionan, o pueden las SV fusionarse en cualquier parte de la membrana del ZA? ¿Están los sitios de fusión de las VA alineados con precisión con los grupos de receptores postsinápticos para garantizar la máxima activación del receptor? ¿Existen diferentes tipos de eventos de transmisión sináptica que transmitan información distinta entre los socios sinápticos?
Esta última pregunta plantea la posibilidad de explicar la manipulación de la transmisión sináptica: se puede transmitir información distinta según el neurotransmisor, su ruta, su sincronización y su receptor. De hecho, un equipo de investigadores de China y Singapur se ha inspirado para imitar la sinapsis en materiales portátiles inteligentes para permitir un flujo de información más eficiente y variable mediante multiplexación, es decir, la transmisión de múltiples tipos de información por el mismo canal de comunicación. ¿Por qué? Porque «la información en las entidades biológicas se transmite mediante portadores de iones solvatados en entornos acuáticos, lo que permite la integración, el paralelismo y un consumo energético óptimo para controlar el movimiento», afirmaron en su artículo publicado en PNAS.
Poda y autoajuste
En Science, Somaiya y Feller escribieron sobre los hallazgos de Matsumoto et al. que revelaron un proceso automático de “poda” durante el desarrollo que optimiza la disposición de las sinapsis:
El funcionamiento de los circuitos neuronales depende de la conexión precisa de las neuronas con sus parejas sinápticas correspondientes. Inicialmente, estas conexiones son imprecisas, ya que las neuronas establecen contacto con múltiples parejas potenciales diferentes. Estas conexiones se vuelven más precisas mediante un proceso llamado poda sináptica, que elimina las sinapsis innecesarias.
Para mí, no basta con citar la Ley de Hebb: «Las nuevas ramas tienden a añadirse en los lugares donde la actividad espontánea de las ramas individuales está más correlacionada con las ondas retinianas, mientras que la actividad asincrónica se asocia con la eliminación de ramas». Algo más controla la sincronización de la actividad; de lo contrario, la poda dejaría solo la rama más fuerte. Un jardinero de rosas sabe cuándo la poda ha sido optimizada para la floración. Algo le indica a una red nerviosa cuándo se ha alcanzado la optimalidad.
Otro artículo en PNAS ofreció razones adicionales para las sinapsis en lugar de las uniones directas. Xiong et al. escribieron sobre el autoajuste de las neuronas presinápticas, incluso en nematodos de baja calidad:
Ante una gran cantidad de desafíos internos y externos, las neuronas muestran una adaptabilidad notable, ajustándose dinámicamente para mantener la estabilidad sináptica y asegurar la fidelidad del funcionamiento del circuito neuronal. Esta adaptabilidad homeostática es esencial no solo para la integridad del circuito neuronal, sino que también tiene implicaciones en diversas patologías psiquiátricas y neurológicas. En la terminal presináptica, el flujo de calcio a través de canales iónicos específicos es necesario para la exocitosis de vesículas sinápticas llenas de neurotransmisores. Nuestros estudios en el nematodo Caenorhabditis elegans revelan un mecanismo sofisticado donde la abundancia de canales de calcio presinápticos está regulada negativamente por la eficiencia de la exocitosis de vesículas sinápticas. Este mecanismo de autorregulación asegura que la liberación de neurotransmisores presinápticos se ajuste de forma autónoma, manteniendo así la función sináptica y salvaguardando la robustez de la comunicación neuronal.
Ahora empiezo a entenderlo. La razón del diseño «torpe» o «chapucero» ─cómo algunos podrían decir─ de la sinapsis es una mayor flexibilidad, flujo de información y adaptabilidad. Y si la transmisión sigue ocurriendo en milisegundos, ¿quién se va a quejar del resultado? Todavía puedo saltar sobre esa roca sin caerme. La vida es buena.
Artículo publicado originalmente por David Coppedge en Evolution News & Science Today
Crédito de la imagen: iStock Photos