Podría decirse que la clase de evidencia más sólida para un diseñador cósmico son los argumentos teleológicos. Está bien establecido que hay muchas más formas en las que podría haber existido el universo que no son propicias para la vida que formas favorables a la vida. Dado el supuesto del teísmo, no es particularmente sorprendente que el universo sea hospitalario para seres conscientes encarnados como nosotros. Por el contrario, dada la suposición del ateísmo, es tremendamente sorprendente que el universo permita la existencia de tales seres. A la luz de esta proporción de probabilidad significativamente elevada, la rareza astronómica de los universos aptos para la vida (y el hecho de que nuestro universo sustenta la vida avanzada) tiende a confirmar el teísmo. Un tipo de argumento teleológico que merece más atención es el argumento basado en la idoneidad ambiental previa de la naturaleza para la existencia de vida avanzada, que ha sido popularizado en los últimos años gracias al trabajo de Michael Denton. En conjunto, la evidencia aducida en los diversos libros de Denton constituye un argumento muy convincente de que detrás del diseño de nuestro universo hay una mente.
Los átomos no metálicos dan forma a las moléculas
Una subclase de evidencia en esta categoría es el aparente ajuste fino de la química para la célula basada en carbono, sobre la cual se puede leer en The Miracle of the Cell [El milagro de la célula], del Dr. Denton.1 Aquí, destacaré sólo un ejemplo. La siguiente figura muestra la tabla periódica de elementos:
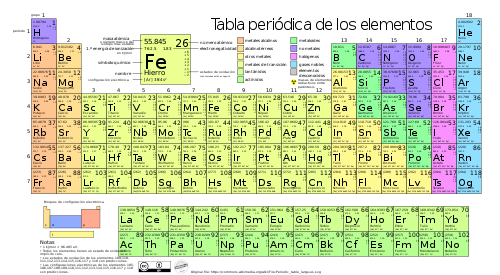
Los elementos coloreados de púrpura en la figura representan los átomos no metálicos, y son estos los que forman las sustancias materiales de la célula, en particular, carbono, hidrógeno, oxígeno y nitrógeno. De hecho, estos son los únicos átomos que podrían usarse para construir un sistema bioquímico, ya que pueden formar enlaces químicos fuertes, estables y direccionales. Fundamentalmente, estos enlaces covalentes dan forma a las moléculas, y es la forma la esencia de la bioquímica.
Fuerza hidrofóbica
Además, estos átomos tienen una electronegatividad tal que la atracción de los electrones por el hidrógeno y el carbono es muy similar. Dado que el carbono y el hidrógeno tienen un valor similar de electronegatividad (es decir, con qué fuerza los átomos atraen los electrones hacia el núcleo), esto significa que pueden compartir electrones por igual entre los dos átomos, creando un enlace covalente no polar. Por otro lado, cuando el oxígeno y el hidrógeno forman un enlace covalente, se obtiene una molécula polar, donde los electrones se comparten de manera desigual (específicamente, el oxígeno tiene un valor de electronegatividad más alto y, por lo tanto, atrae a los electrones compartidos en el enlace con más fuerza que el hidrógeno).
Esto es fundamental para toda la organización de la célula, porque le proporciona la fuerza hidrofóbica, que es responsable de organizar la estructura superior del ámbito biológico. La fuerza hidrofóbica se refiere a la tendencia de las sustancias no polares a agregarse en un ambiente acuoso para minimizar su exposición al agua. ¿Qué causa este efecto? Cuando se introducen moléculas no polares en el agua, se altera la red estructurada de enlaces de hidrógeno del agua. Las moléculas de agua no pueden formar enlaces de hidrógeno con moléculas apolares, lo que conduce a una situación energéticamente desfavorable. Para minimizar esta alteración, las moléculas de agua se organizan de tal manera que puedan mantener tantos enlaces de hidrógeno como sea posible. Para reducir el costo entrópico y aumentar la estabilidad general, las moléculas no polares tienden a agregarse. Al agruparse de esta manera, se minimiza la superficie en contacto con el agua y esto reduce la cantidad de moléculas de agua que necesitan reorganizarse a su alrededor. Por esta razón, las moléculas no polares también se denominan “hidrófobas” (repelen el agua), mientras que las moléculas polares se denominan “hidrófilas” (atraen el agua).
La fuerza hidrofóbica es crucial para el ensamblaje de membranas y proteínas. Las membranas biológicas están formadas por fosfolípidos, que poseen cabezas hidrófilas y colas hidrófobas. Las colas hidrófobas evitan el contacto con el agua, mientras que las cabezas hidrófilas interactúan con ella. El resultado es el autoensamblaje de los fosfolípidos en una bicapa con las colas hacia adentro y las cabezas hacia afuera. De manera similar, en una estructura proteica, las cadenas laterales de aminoácidos que son hidrófobas tienden a evitar el contacto con el entorno acuoso. Por otro lado, los grupos químicos asociados con cadenas laterales polares (hidrófilas) como los grupos hidroxilo (-OH), amina (-NH2) y carboxilo (-COOH) forman enlaces de hidrógeno con el agua. La fuerza hidrofóbica impulsa los residuos no polares hacia el interior de la proteína, mientras que los residuos polares quedan expuestos en la superficie, interactuando con el agua. Esto conduce al plegamiento espontáneo de la proteína en su estructura tridimensional nativa, lo cual es crucial para su función.
Tan crucial es la fuerza hidrofóbica para el plegamiento de las proteínas que el bioquímico Charles Tanford, al describir el descubrimiento de cómo se pliegan las proteínas, señala que “[L]a fuerza hidrofóbica es la fuerza energéticamente dominante para la contención, la adhesión, etc., en todos los procesos de la vida… Esto significa que toda la naturaleza de la vida tal como la conocemos es esclava de la estructura de enlaces de hidrógeno del agua líquida”.2
Una coincidencia fortuita
Por tanto, es una coincidencia notablemente fortuita que los mismos átomos que producen formas estables y definidas (a partir de las cuales se pueden construir macromoléculas) también generen la fuerza hidrofóbica que es la clave para ensamblarlos en formas tridimensionales superiores. La naturaleza no nos debe esta convergencia favorable a la vida y, sin embargo, si no fuera por esta coincidencia, la vida no podría existir. Ésta es sólo una de muchas coincidencias similares que son cruciales para la existencia de la vida y, en particular, de la vida avanzada. En conjunto, la evidencia sugiere que el universo fue diseñado teniendo en mente la vida.
Notas
- Michael Denton, The Miracle of the Cell (Discovery Institute Press, 2020).
- Charles Tanford, “How Protein Chemists learned about the Hydrophobic Factor: Protein Chemists and the Hydrophobic Factor.” Protein Science, vol. 6, no. 6, 1997, 1358-1366.
Artículo publicado originalmente en inglés por Jonathan McLatchie Ph.D. en Evolution News & Science Today