Recientemente, se obtuvieron datos de composición química de muestras recuperadas por la nave espacial japonesa Hayabusa2 que aterrizó en dos ubicaciones en el asteroide (162173) Ryugu. En diciembre de 2020, Hayabusa2 regresó con éxito a la Tierra con sus preciosas muestras prístinas, no contaminadas por residuos de la Tierra (excepto tal vez algún material metálico procedente del dispositivo de recolección). Publicado en Science, los primeros análisis de compuestos orgánicos extraídos de las muestras recolectadas incluyeron mezclas significativamente racémicas de varios aminoácidos, lo que indica que estas muestras estaban relativamente libres de contaminación terrestre de biopolímeros.1 (Todas las proteínas en la vida están hechas de L-amino racémicamente puro ácidos.) Los análisis previos de meteoritos no podían jactarse de tal pureza no contaminados por los productos biológicos de la Tierra.
Por lo tanto, estas muestras de Ryugu parecen ser nuestra primera oportunidad de examinar qué compuestos orgánicos se pueden producir en un entorno prebiótico en nuestro sistema solar. Además, no tenemos que confiar en estimaciones inciertas de las condiciones en la Tierra cuando se estaba formando el sistema solar. Los asteroides que contienen cantidades significativas de carbono, nunca visitados por extraterrestres como nosotros, pueden proporcionar una idea razonable de lo que puede producir la química abiótica.
¿Vino del espacio exterior?
Un artículo reciente en Nature Communications informó que se identificó uracilo, una de las nucleobases que se encuentran en el ARN, en estas muestras prístinas de Ryugu.2 Para aquellos que apuestan por la hipótesis del mundo del ARN, este es un hallazgo significativo, al menos en su opinión. . Finalmente tienen evidencia de que al menos una de las nucleobases del ARN ha sido descubierta fuera de la Tierra, por lo tanto, dicen, ¡mantienen la idea de que nuestra bioquímica podría haber sido sembrada desde el espacio exterior! Como resume WordsSideKick.com: «Después de quedar atrapadas en asteroides como Ryugu, es posible que estas moléculas finalmente hayan llegado a la Tierra a través de impactos de meteoritos, donde provocaron los primeros indicios de vida en los océanos primordiales».
Esta puede ser nuestra primera oportunidad de comentar sobre datos válidos de productos químicos prebióticos libres de contaminación terrestre. Por lo tanto, sería lógico considerar primero el análisis químico inicial descrito en Science para clasificar ampliamente todos los compuestos orgánicos, identificados mediante dos métodos analíticos sensibles. En cuanto a los componentes básicos de la vida, encontraron varios aminoácidos, pero todos en mezclas racémicas. Esto es precisamente lo que predicen los químicos. Es extremadamente difícil producir compuestos ópticamente puros a partir de compuestos más pequeños. La química de los compuestos reflejados en el espejo es exactamente la misma, y solo difieren en la orientación espacial de los átomos unidos covalentemente (análogo a que sus manos derecha e izquierda sean equivalentes). La vida solo usa una de estas formas químicas para producir proteínas, ARN, ADN, carbohidratos complejos y muchos lípidos.
Solo los aminoácidos más simples
En Ryugu solo se detectaron algunos de los aminoácidos más simples, incluidos glicina, D/L-alanina, D/L-serina y D/L-valina, junto con otros aminoácidos que no se usan para construir proteínas (Fig. 1). Estos resultados concuerdan bien con los experimentos anteriores de Stanley Miller y otros en los que se produjeron fácilmente estructuras orgánicas simples en simulaciones prebióticas. Sin embargo, más de ocho aminoácidos con grupos funcionales críticos más complejos aún no han resultado entre las diversas permutaciones de reacciones prebióticas probadas. No es solo tratar con mezclas racémicas lo que confunde a los partidarios de la abiogénesis, sino cómo formar esos aminoácidos más elaborados cuyas cadenas laterales juegan un papel crítico en la actividad y estructura de todas las proteínas.
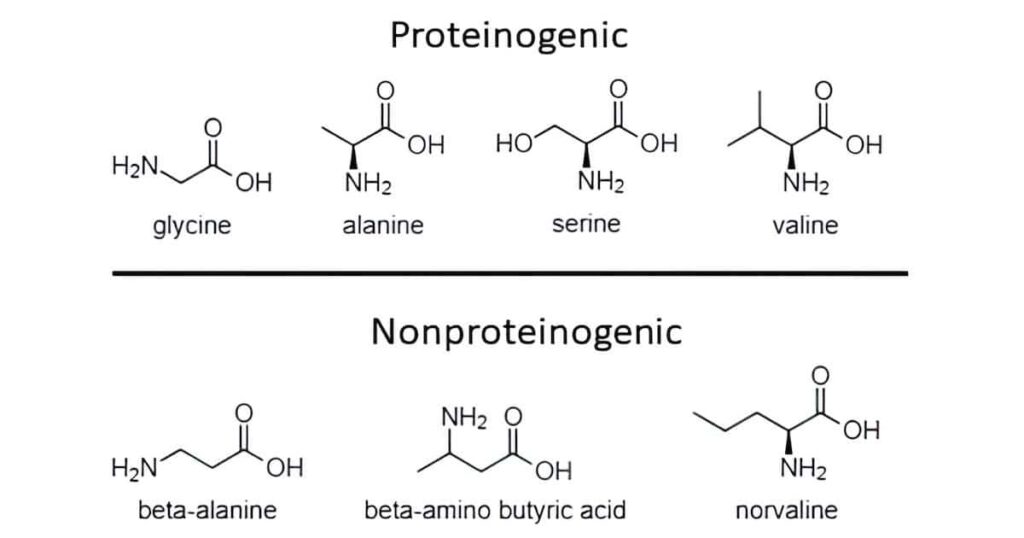
Fig. 1. Estructuras químicas de los cuatro aminoácidos identificados de Ryugu que coinciden con los que se encuentran en las proteínas más ejemplos de tres aminoácidos (entre 11) que no se encuentran en las proteínas.
El análisis químico también reportó miles de compuestos orgánicos, clasificados en múltiples grupos, que pueden o no encontrarse en el contexto de los organismos vivos. Si se originara una sopa primordial a partir de esta mezcla, cualquier biomolécula tendría que lidiar con una miríada de posibles reacciones secundarias con una variedad de compuestos reactivos que compiten por los derechos para producir un biopolímero. ¿Sería diferente la situación si el material del asteroide simplemente sembrara la Tierra con estos bloques de construcción necesarios? Los contaminantes que compiten aún superan en número a las moléculas biológicamente relevantes.
La ruta del ARN
Consideremos si las perspectivas son mejores si tomamos la ruta del ARN. Uracil fue claramente identificado por Ryugu. El umbral de ingeniería para formar nucleótidos, los componentes básicos del ARN, es mucho más alto que el de las proteínas. La unidad central a la que se unen las nucleobases y el fosfato es el azúcar D-ribosa de 5 carbonos. Se han propuesto varios mecanismos para explicar cómo los carbohidratos pueden haberse originado en un ambiente abiótico.3 Los desafíos para integrar la D-ribosa en los nucleótidos de manera abiótica se pueden resumir en tres barreras químicas principales. 1) La producción abiótica de azúcares de cinco carbonos producirá cuatro estereoisómeros químicamente equivalentes en las formas D y L, lo que da como resultado ocho estereoisómeros en niveles aproximadamente iguales (Fig. 2A). ¿Cómo se selecciona la D-ribosa a través de la química aleatoria sin siquiera considerar que también estarán presentes azúcares de cadena más larga? 2) La ribosa puede interconvertirse de una forma de cadena abierta a una estructura de anillo de seis miembros (forma de piranosa) o a un anillo de cinco miembros (furanosa), los cuales se presentan como configuraciones alfa y beta en el carbono 1 (Fig. 2B) . En el equilibrio, la forma de piranosa comprende el 80 por ciento, mientras que la forma de furanosa es el 20 por ciento de la ribosa. El ARN usa la forma de furanosa, entonces, ¿cómo gana este componente menor en cualquier reacción abiótica? 3) El nitrógeno en la posición 1 del uracilo debe unirse al carbono 1 de la D-ribosa en una configuración beta a través de una reacción termodinámicamente desfavorable. ¿Cómo puede ocurrir esta reacción abióticamente?
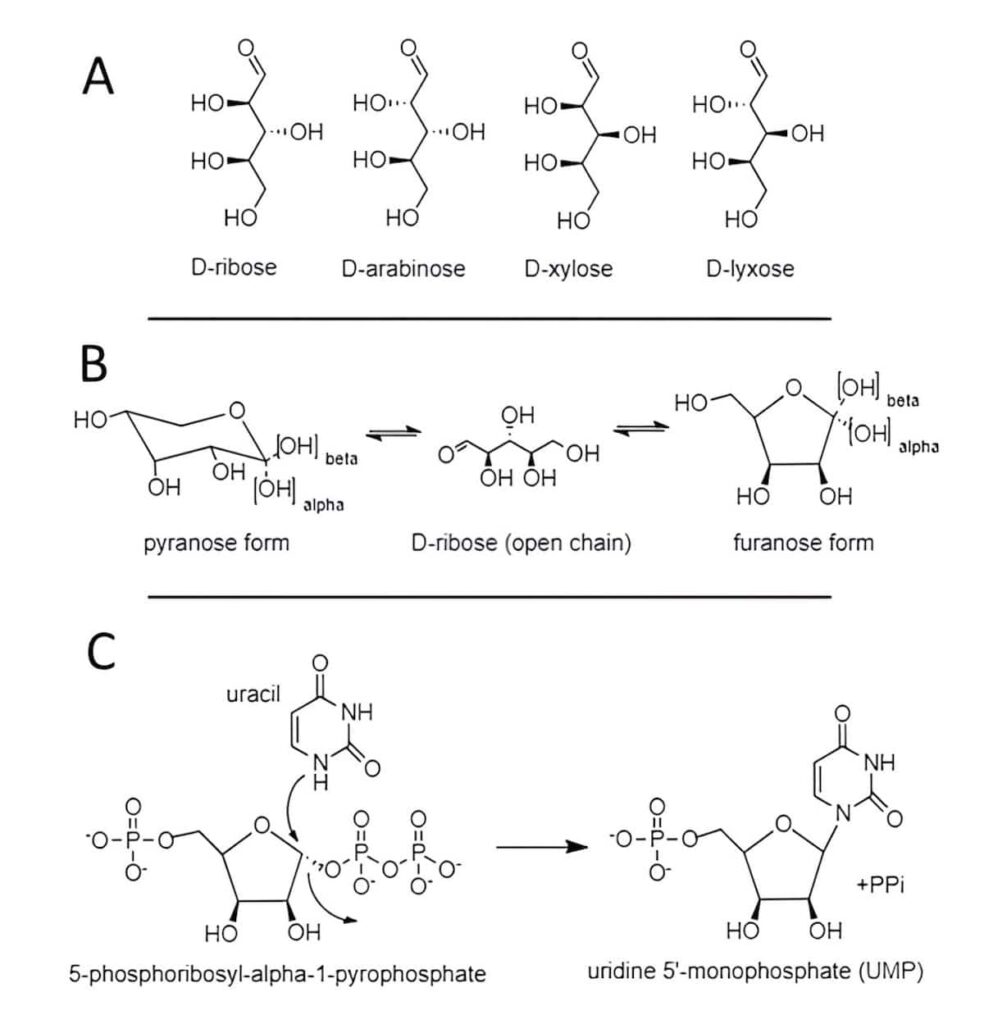
Fig. 2 Química de azúcares de 5 carbonos. A. Las estructuras de las cuatro D-pentosas se muestran con proyecciones estereoquímicas (las barras en negrita son enlaces que se extienden hacia el espectador mientras que las barras sombreadas se extienden hacia afuera). Tenga en cuenta las diferencias en las orientaciones espaciales de todos los grupos hidroxilo (OH). Los azúcares L son simplemente las imágenes especulares de estas estructuras que representan un total de ocho estereoisómeros. B. Interconversión de D-ribosa entre estructuras de anillo de piranosa y furanosa. Los arreglos de las configuraciones alfa y beta se indican mediante líneas discontinuas en el carbono 1. El ARN usa solo la forma de furanosa con la nucleobase unida en la configuración beta. C. Acoplamiento enzimático de uracilo a ribosa 5-fosfato. La enzima posiciona ambos sustratos apropiadamente para catalizar este desplazamiento estereoespecífico formando un nuevo enlace químico.
Ignorando los enigmas
Si bien los dos primeros acertijos suelen ser eludidos por quienes defienden la filosofía del mundo del ARN, la última reacción no es una tarea imposible, por lo que consideraremos cómo la vida logra esta hazaña. La mayoría de las células pueden recuperar bloques de construcción de ARN o ADN que normalmente se obtienen nutricionalmente después de la digestión. Las nucleobases liberadas pueden acoplarse utilizando D-ribosa cargada con un grupo pirofosfato en el carbono 1 en configuración alfa. Observe los usos específicos de la vida donde ni la configuración beta ni la forma del anillo de piranosa funcionarán para esta reacción. Este sustrato permite un enfoque específicamente orientado por el nitrógeno apropiado de la base nitrogenada, dirigido completamente por la enzima respectiva, para efectuar el desplazamiento del pirofosfato. Esto da como resultado que la nucleobase se una al carbono 1 en la configuración beta (Fig. 2C). La liberación de pirofosfato cumple con los requisitos termodinámicos de esta elaborada reacción.
Se han hecho intentos para llevar a cabo esta reacción en condiciones supuestamente abióticas. Estos esfuerzos condujeron a una planificación ingeniosa para idear nuevos esquemas químicos sintéticos que involucran electropulverización de microgotas que contienen D-ribosa, fosfato y nucleobases.4 Los investigadores proporcionan evidencia que propone cómo las microgotas podrían favorecer termodinámicamente esta reacción. Es factible que los cuatro nucleótidos se produzcan a través de esta ruta.
Otras preocupaciones graves
Pero este informe no abordó las otras preocupaciones graves ya discutidas. Usaron D-ribosa pura, no una mezcla de azúcares como se esperaría prebióticamente, y mínimamente no D/L-ribosa. La configuración alfa/beta de los productos, o sus estructuras de anillo, no se indicaron (muy probablemente resultando en mezclas de todos los productos posibles). Por lo tanto, se vuelve difícil evaluar la relevancia de esta reacción para producir bloques de construcción de ARN biológicamente viables. Finalmente, los rendimientos de los productos deseados por este mecanismo fueron bajos, del 2,5 por ciento o menos. Si bien el intento de producir bloques de construcción de ARN a través de un mecanismo abiótico es digno de aplauso, esto todavía está muy por debajo de lo que la vida necesita para comenzar a partir de la compleja mezcla de compuestos orgánicos presentes en un mundo prebiótico.
Se alienta a los lectores a investigar más a fondo para comprender mejor los difíciles problemas involucrados en la formación de la vida utilizando solo la química orgánica aleatoria. El químico Dr. James Tour de la Universidad de Rice, por su parte, ha abordado la abiogénesis incluso en debates en su canal de YouTube. Véase también su capítulo en el libro de descarga gratuita Science and Faith in Dialogue.
Notas
- Naraoka H, Takano Y, Dworkin JP, Oba Y, Hamase K, Furusho A, et al. Soluble organic molecules in samples of the carbonaceous asteroid (162173) Ryugu. Science 2023; 379(6634):eabn9033 doi 10.1126/science.abn9033.
- Oba Y, Koga T, Takano Y, Ogawa NO, Ohkouchi N, Sasaki K, et al. Uracil in the carbonaceous asteroid (162173) Ryugu. Nat Commun 2023; 14(1):1292 doi 10.1038/s41467-023-36904-3.
- Yadav M, Kumar R, Krishnamurthy R. Chemistry of Abiotic Nucleotide Synthesis. Chemical Reviews 2020; 120(11):4766-805 doi 10.1021/acs.chemrev.9b00546.
- Nam I, Nam HG, Zare RN. Abiotic synthesis of purine and pyrimidine ribonucleosides in aqueous microdroplets. Proc Natl Acad Sci U S A 2018; 115(1):36-40 doi 10.1073/pnas.1718559115.
Artículo publicado originalmente en inglés por Carl Linnaeus (seudónimo) en Evolution News & Science Today